Un ácido es una solución que tiene un exceso de hidrógeno (H +) iones. Una base es una solución que tiene un exceso de hidróxido (OH-) los iones.
Cuando en una solución la concentración de iones hidrógeno (H+)es mayor que la de iones hidróxilo (OH–), se dice que es ácida. En cambio, se llama básica o alcalina a la solución cuya concentración de iones hidrógeno es menor que la de iones hidróxilo.
Una solución es neutra cuando su concentración de iones hidrógeno es igual a la de iones hidróxilo. El agua pura es neutra porque en ella [H+] = [OH–]. (Ver: Ionización del agua)
La primera definición de ácido y base fue acuñada en la década de 1880 por Savane Arrhenius quien los define como sustancias que pueden donar protones (H+) o iones hidróxido (OH-), respectivamente. Esta definición es por supuesto incompleta, pues existen moléculas como el amoniaco (NH3) que carecen del grupo OH- y poseen características básicas.
 |
Una definición más general fue propuesta en 1923 por Johannes Brönsted y Thomas Lowry quienes enunciaron que una sustancia ácida es aquella que puede donar H+, exactamente igual a la definición de Arrhenius; pero a diferencia de éste, definieron a una base como una sustancia que puede aceptar protones.
Una definición más general sobre ácidos y bases fue propuesta por Gilbert Lewis quien describió que un ácido es una sustancia que puede aceptar un par de electrones y una base es aquella que puede donar ese par.
Los ácidos y las bases se caracterizan por:
Ácidos
|
Bases
|
| Tienen sabor agrio (limón, vinagre, etc). | Tiene sabor cáustico o amargo (a lejía) |
| En disolución acuosa enrojecen la tintura o papel de tornasol | En disolución acuosa azulean el papel o tintura de tornasol |
| Decoloran la fenolftaleína enrojecida por las bases | Enrojecen la disolución alcohólica de la fenolftaleína |
| Producen efervescencia con el carbonato de calcio (mármol) | Producen una sensación untuosa al tacto |
| Reaccionan con algunos metales (como el cinc, hierro,…), desprendiendo hidrógeno | Precipitan sustancias disueltas por ácidos |
| Neutralizan la acción de las bases | Neutralizan la acción de los ácidos |
| En disolución acuosa dejan pasar la corriente eléctrica, experimentando ellos, al mismo tiempo una descomposición química | En disolución acuosa dejan pasar la corriente eléctrica, experimentando ellas, al mismo tiempo, una descomposición química |
| Concentrados destruyen los tejidos biológicos vivos (son corrosivos para la piel) | Suaves al tacto pero corrosivos con la piel (destruyen los tejidos vivos) |
| Enrojecen ciertos colorantes vegetales | Dan color azul a ciertos colorantes vegetales |
| Disuelven sustancias | Disuelven grasas y el azufre |
| Pierden sus propiedades al reaccionar con bases | Pierden sus propiedades al reaccionar con ácidos |
| Se usan en la fabricación de jabones a partir de grasas y aceites |
Tanto ácidos como bases se encuentran en gran cantidad en productos usados en la vida cotidiana, para la industria y la higiene, así como en frutas y otros alimentos, mientras que el exceso o defecto de sus cantidades relativas en nuestro organismo se traduce en problemas de salud.
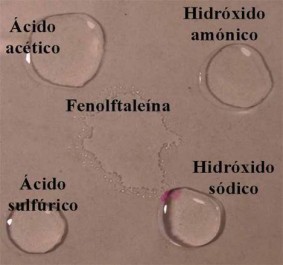 | 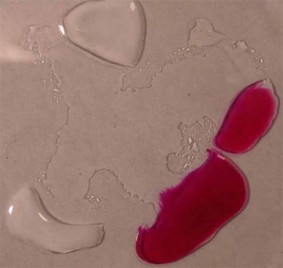 |
| Cómo reacciona una gota de fenolftaleína al unirse con ácidos o con bases. | |
Teoría Ácido-Base de Lowry-Bronsted
Según Bronsted y Lowry, ácidos son todos los compuestos o iones capaces de ceder protones (H+) al medio y bases son los que pueden aceptar protones del medio.
Cuando una molécula o anión puede tomar un H+ (base de Bronsted-Lowry), se forma su "ácido conjugado"
Base
|
Protón que gana
|
Ácido conjugado
|
OH-
|
H+
|
H2O
|
NH3
|
H+
|
NH4+
|
CO3-2
|
H+
|
CO3H-
|
Cuando un ácido pierde un ion hidrógeno, se forma su "base conjugada".
Ácido
|
Protón que pierde
|
Base conjugada
|
ClH
|
H+
|
Cl-
|
SO4H2
|
H+
|
SO4H-
|
NO3H
|
H+
|
NO3-
|
Fuerza de los ácidos y las bases
La fuerza de un ácido o la de una base está determinada por su tendencia a perder o a ganar protones. Los ácidos pueden dividirse en fuertes (ClH, SO4H2, NO3H, etc.) y débiles (PO4H2–, CH3COOH, CO3H2, etc.). Las moléculas de los primeros se disocian en forma prácticamente total al ser disueltos en agua. Los segundos sólo ionizan una pequeña proporción de sus moléculas. De aquí que, para una misma concentración de ácido, la concentración de iones hidrógeno es mayor en las soluciones de ácidos fuertes que en las de los débiles.
Las bases también pueden dividirse en fuertes (NaOH, KOH, Ca (OH)2, etc.) y débiles (NH3, trimetilamina, anilina, etc.). Las primeras se disocian completamente en solución. Al igual que para ácidos débiles, las constantes de disociación de las bases débiles (KB) reflejan el grado de ionización.
Una generalización útil acerca de las fuerzas relativas de los pares ácido-base es que si un ácido es fuerte, su base conjugada es débil y, para las bases, si una sustancia es una base fuerte, su ácido conjugado es débil.
La Neutralización
Tal como puede ver arriba, los ácidos sueltan H+ en la solución y las bases sueltan OH-. Si fuésemos a mezclar un ácido y una base, el ión H+ se combinaría con el ión OH-ion para crear la molécula H2O, o simplemente agua:
H+(aq)
|
+
|
OH-(aq)
|
H2O
|
La reacción neutralizante de un ácido con una base siempre producirá agua y sal, tal como se muestra abajo:
Ácido
|
Base
|
Agua
|
Sal
| |||
HCl
|
+
|
NaOH
|
H2O
|
+
|
NaCl
| |
HBr
|
+
|
KOH
|
H2O
|
+
|
KBr
|
Aunque Arrhenius ayudó a explicar los fundamentos de la química sobre ácidos ybases, lastimosamente sus teorías tenían límites. Por ejemplo, la definición de Arrhenius no explica por qué algunas substancias como la levadura común (NaHCO3) puede actuar como una base, a pesar de que no contenga iones de hidrógeno.
En 1923, el científico danés Johannes Brønsted y el inglés Thomas Lowry publicaron diferentes aunque similares trabajos que redefinieron la teoría de Arrhenius. En las palabras de Brønsted's words, "... los ácidos y las bases son substancias que tiene la capacidad de dividirse o tomar iones de hidrógeno respectivamente." La definición de Brønsted-Lowry ampliar el concepto de Arrhenius sobre los ácidos y las bases.
La definición de Brønsted-Lowry sobre los ácidos es muy similar a la de Arrhenius, cualquier substancia que pueda donar un ión de hidrógeno, es un ácido (en la definición de Brønsted, los ácidos son comúnmente referidos como donantes de protones porque un ión- hidrógeno H+ menos su electrón - es simplemente un protón).
Sin embargo, la definición de Brønsted de las bases es bastante diferente de la definición de Arrhenius. La base de Brønsted es definida como cualquier substancia que puede aceptar un ión de hidrógeno. Esencialmente, la base es el opuesto de un ácido. El NaOH y el KOH, tal como vimos arriba, seguirían siendo consideradas bases porque pueden aceptar un H+ de un ácido para formar agua. Sin embargo, la definición de Brønsted-Lowry también explica por que las substancias que no contienen OH- pueden actuar como bases. La levadura (NaHCO3), por ejemplo, actúa como una base al aceptar un ión de hidrógeno de un ácido tal como se ilustra siguientemente:
Acido
|
Base
|
Sal
| ||||
HCl
|
+
|
NaHCO3
|
H2CO3
|
+
|
NaCl
|
En este ejemplo, el acido carbónico formado (H2CO3) pasa por descomposición rápida a agua y dióxido de carbono gaseoso, y también las burbujas de solución como el gas CO2 se liberan.
pH
En la definición de Brønsted-Lowry, ambos los ácidos y las bases están relacionados con la concentración del ión de hidrógeno presente. Los ácidos aumentan la concentración de iones de hidrógeno, mientras que las bases disminuyen en la concentración de iones de hidrógeno (al aceptarlos). Por consiguiente, la acidez o la alcalinidad de algo puede ser medida por su concentración de iones de hidrógeno.
En 1909, el bioquímico danés Sören Sörensen inventó la escala pH para medir la acidez. La escala pH está descrita en la fórmula:
|
Por ejemplo, una solución con [H+] = 1 x 10-7 moles/litro tiene un pH = 7 (una manera más simple de pensar en el pH es que es igual al exponente del H+ de la concentración, ignorando el signo de menos). La escala pH va de 0 a 14. Las substancias con un pH entre S 0 o menos de 7 son ácidos (pH y [H+] están inversamente relacionados, menor pH significa mayor [H+]). Las substancias con un pH mayor a 7 y hasta 14 son bases (mayor pH significa menor [H+]). Exactamente en el medio, en pH = 7, están las substancias neutra s, por ejemplo, el agua pura. La relación entre [H+] y pH está mostrada en la tabla de abajo, junto algunos comunes ejemplos de ácidos y base de la vida cotidiana.
[H+]
|
pH
|
Ejemplo
| |
Ácidos
|
1 X 100
|
0
|
HCl
|
1 x 10-1
|
1
|
Ácido estomacal
| |
1 x 10-2
|
2
|
Jugo de limón
| |
1 x 10-3
|
3
|
Vinagre
| |
1 x 10-4
|
4
|
Soda
| |
1 x 10-5
|
5
|
Agua de lluvia
| |
1 x 10-6
|
6
|
Leche
| |
Neutral
|
1 x 10-7
|
7
|
Agua pura
|
Bases
|
1 x 10-8
|
8
|
Claras de huevo
|
1 x 10-9
|
9
|
Levadura
| |
1 x 10-10
|
10
|
Tums®antiácidos
| |
1 x 10-11
|
11
|
Amoníaco
| |
1 x 10-12
|
12
|
Caliza Mineral - Ca(OH)2
| |
1 x 10-13
|
13
|
Drano®
| |
1 x 10-14
|
14
|
NaOH
|
Escala de pH
Para cuantificar el carácter ácido o básico de una sustancia empleamos la escala de pH, que es una escala de números del 1 a 14.
- Si el pH es menor que 7, la sustancia es ácida. Ejemplo: disolución de cloruro de hidrógeno (ácido clorhídrico) en agua.
- Si el pH es mayor que 7, la sustancia es básica. Ejemplo: disolución de hidróxido de sodio (sosa) en agua.
- Si el pH es igual a 7, entonces la sustancia es neutra. Ejemplo: el agua.
Esta escala de números se asocia a una escala de colores. Estos colores son los que adopta el papel indicador en contacto con el ácido o la base.

¿Qué es un indicador ?
Los indicadores son colorantes orgánicos, que cambian de color según estén en presencia de una sustancia ácida, o básica.
Fabricación casera de un indicador
Las lombardas, parecidas a repollos y de color violeta, contienen en sus hojas un indicador que pertenece a un tipo de sustancias orgánicas denominadas antocianinas.Para extraerlo :
-
Corta unas hojas de lombarda (cuanto más oscuras mejor)
-
Cuécelas en un recipiente con un poco de agua durante al menos 10 minutos
-
Retira el recipiente del fuego y dejarlo enfriar
-
Filtra el líquido (Se puede hacer con un trozo de tela vieja)
-
Ya tienes el indicador (El líquido filtrado)
Corta unas hojas de lombarda (cuanto más oscuras mejor)
Cuécelas en un recipiente con un poco de agua durante al menos 10 minutos
Retira el recipiente del fuego y dejarlo enfriar
Filtra el líquido (Se puede hacer con un trozo de tela vieja)
Ya tienes el indicador (El líquido filtrado)
Ácidos Orgánicos
Los ácidos orgánicos son un grupo de sustancias generalmente no se disuelven en agua sino en disolventes orgánicos. Reaccionan con ciertos metales desprendiendo hidrógeno. Aunque en su molécula existen varios hidrógenos, solo son capaces de ceder los que se encuentran unidos en un grupo OH ( del carboxilo R-COOH, del sulfónico R-SO3 H o de los fenoles R- OH). A continuación se describen algunos pares ácido-base:
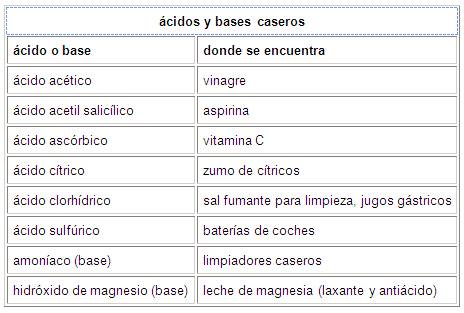
En la tabla que sigue aparecen algunos ácidos y bases corrientes :
No hay comentarios:
Publicar un comentario